올해 2월 임상을 중단하라는 명령을 받았던 펄크럼이, 마침내 임상시험을 재개하는데 성공했습니다.

겸상적혈구빈혈을 표적으로 하는 FTX-6058의 임상 1b상이었고, 이번 임상 재개로 인해 회사는 SCD 치료를 위한 경구용 억제제 개발에 한발을 더 내딛었습니다.
SCD란?
겸상적혈구빈혈(sickle cell disease, SCD)은 HBB 유전자의 변이로 인해 발생하는 적혈구 질환입니다.
HBB는 헤모글로빈의 핵심 단백질을 만드는 유전자이기에, 해당 변이로 결국 산소 운반 효율이 떨어지고, 낫 모양(=겸상)의 적혈구가 형성됩니다.
이 낫 모양 적혈구들은 서로 쉽게 엉켜서 혈관을 막거나 세포를 파열시키기도 하는데,
이로 인해 빈혈, 통증, 감염, 뇌졸중, 심장병, 폐고혈압, 신부전, 간 질환, 기대 수명 감소 등 심각한 증상을 앓게 됩니다.
FTX-6058의 작용기전
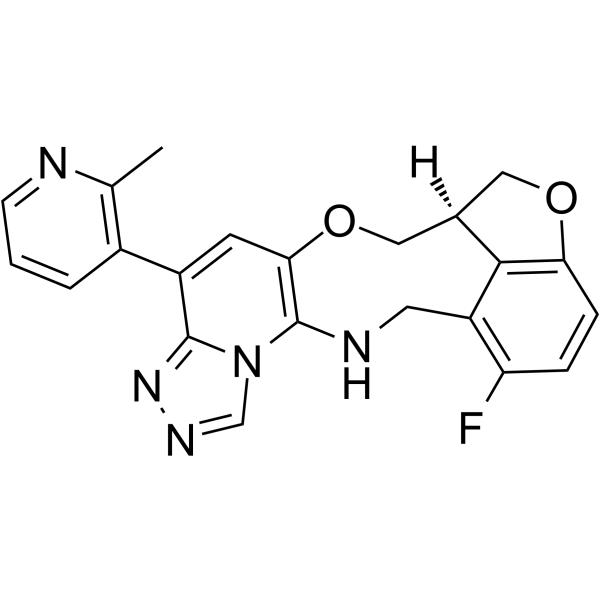
FTX-6058은 태아 헤모글로빈 (fetal hemoglobin, HbF)라는 물질을 증가시키는 약물입니다.
일반적인 헤모글로빈보다 산소 결합력이 좋고(약 300배), 원래는 출생 이후 점점 사라지는 물질입니다.
그런데 이 HbF를 다시금 생산하도록 유도해서 정상적혈구의 분포를 개선하고, 산소 운반을 활성화시킵니다.
이 과정을 위해 FTX-6058은 PRC2 복합체의 일부인 EED라는 물질을 억제하고, 이것이 BCL11A를 포함한 여러 HbF의 억제인자의 발현을 낮춥니다.
FTX-6058은 전임상 연구에서 태아 헤모글로빈이 증가한다는 사실을 실제로 입증했습니다.
임상시험 현황
이후 회사는 20년에 진행한 임상 1a에서 (NCT04586985) 건강인과 SCD환자 모두를 대상으로 효과적으로 임상을 완료했었고,
이후 21년부터 1b상을 진행하게 됩니다. (NCT05169580)
[임상디자인]
이번 1b 임상은 SCD 환자를 대상으로 진행되며,
코호트별 10명씩, 저용량 (6mg)과 고용량 (20mg)을 q.d.로 4주동안 복용합니다.
이 때 안전성, 내약성, PK등의 지표를 확인합니다.
- 지표에 따라 추가 코호트를 구성할 수 있는 형태입니다.
[임상결과]
회사는 dose dependent하게 HbF 수치가 증가함을 확인했었습니다.
6mg 저용량에서 HbF의 절대량이 기준치보다 9.5% 증가했습니다.
또한 최대 3개월간 노출된 환자에서 내약성은 양호했고, 치료관련 심각한 부작용은 없었습니다.
1b 임상시험의 중단
그런데 FDA에서 동물임상 데이터 검토 후 임상보류를 요청합니다.
PRC2를 억제하는 다른약에서 혈액암 가능성이 제기되었기 때문이죠.
FDA가 직접 "사전에 보고된 전임상 데이터에 문제가 있다"고 지적을 했고, 결국 FDA는 위험을 감수할 만큼 치료효과가 큰 집단을 다시 찾을 것을 요청했습니다.
어떻게 보면 임상시험보다는 전임상 결과에 따른 문제였죠.
PRC2 표적 약물의 문제점
이번 이슈는 FTX-6058이 표적하는 PRC2(polycomb repressive complex 2)가 시작이었습니다.
해당 표적을 억제하면 2차로 혈액암을 유발할 수 있다는 결과가 있기 때문이죠.
- PRC2는 H3K27이라는 히스톤을 methylation 시키는 효소로 알려져 있습니다.
대표적인 약물이 에피자임의 타즈베릭(Tazverik, tazemetostat)입니다.
타즈베릭은 20년에 상피양 육종(epithelioid sarcoma) 치료제로 승인받은 약물인데, 이 약물이 PRC2의 EZH2라는 또다른 subunit을 표적합니다.
- PRC2는 FTX-6058이 표적하는 EED, 타즈베릭이 표적하는 EZH2등이 모여서 이루는 복합체죠.
- 타즈베릭은 20년 6월, 여포성 림프종(follicular lymphomas)으로 적응증이 확대되기도 했습니다.

그런데, 이 약물은 라벨에 혈액암에 대한 경고문구가 부착되어있습니다.
실제로 타즈베릭으로 치료받은 환자는 T세포림프모구림프종(T-LBL), 골수형성이상증후군(MDS), 급성골수성백혈병(AML) 등의 혈액암에 걸릴 위험이 더 높기 때문입니다.
그럼에도, FDA가 이번에 임상시험을 풀어주었고,
결과적으로 동물실험에서 결과를 보았을 때, 암의 발병 가능성보다 질환의 치료가 더 중요하다고 판단된 것으로 보입니다.
SCD의 유전자 치료제 개발이 뜨거운 가운데, 편의성이 강조된 소분자 화합물 역시 개발노력이 지속되고 있습니다.
기타 사항
FTX-6058은 미국 식품의약국(FDA)으로부터 SCD 치료를 위한 패스트 트랙 지정 및 희귀의약품 지정을 받은 상황입니다. 또한 이번 발표로 펄크럼의 주가는 하루만에 약 30% 상승했습니다.

![[특집] 알츠하이머를 크리스퍼 편집기술로 치료할 수 있을까?의 썸네일 이미지](https://cdn.maily.so/202308/bioglobe/1692665728973250.jpg)