현재 가장 앞서있는 유전자 편집기술로 알려진 CRISPR/Cas9으로 알츠하이머를 치료하려는 움직임이 빨라지고 있습니다.

그런 가운데, 아직 극복해야할 장벽이 많다는 입장도 존재합니다.
이번에 AAIC에서 발표된 2가지 치료 사례와 이에 대한 지적을 biospace에서 마련한 특집기사를 중심으로 살펴봅니다.
APP 편집을 통한 알츠하이머 치료
UCSD의 브렌트 얼스턴(Brent Aulston) 연구팀은 CRISPR를 사용하여 아밀로이드 전구체(amyloid precursor protein, APP)를 편집하고 있습니다.
이들의 목적은 APP의 기능은 온전히 유지하면서, β-secretase에 잘리지 않게 하는 것이라 볼 수 있습니다.
- APP는 중요한 기능을 하기 때문에 함부로 편집/제거할 수 없습니다. 뇌 및 신경성장, 염증반응, 인지능력 등에 영향을 주는 것으로 알려져 있죠.
- 또한 APP는 주로 α와 β-secretase에 의해 분해되는데, β-secretase에 잘리면 amyloid-β (Aβ)가 되기 때문에 β-secretase와의 접촉을 줄여야 합니다.
- 반면 α-secretase와 접촉하면 정상적으로 절단되어 APP-α라는 정상 단백질을 발현합니다.
실험팀은 amyloid-β (Aβ) 발현은 줄이면서 APP-α 발현은 증가, 임상적인 증상도 같이 개선되는 것을 확인했습니다.
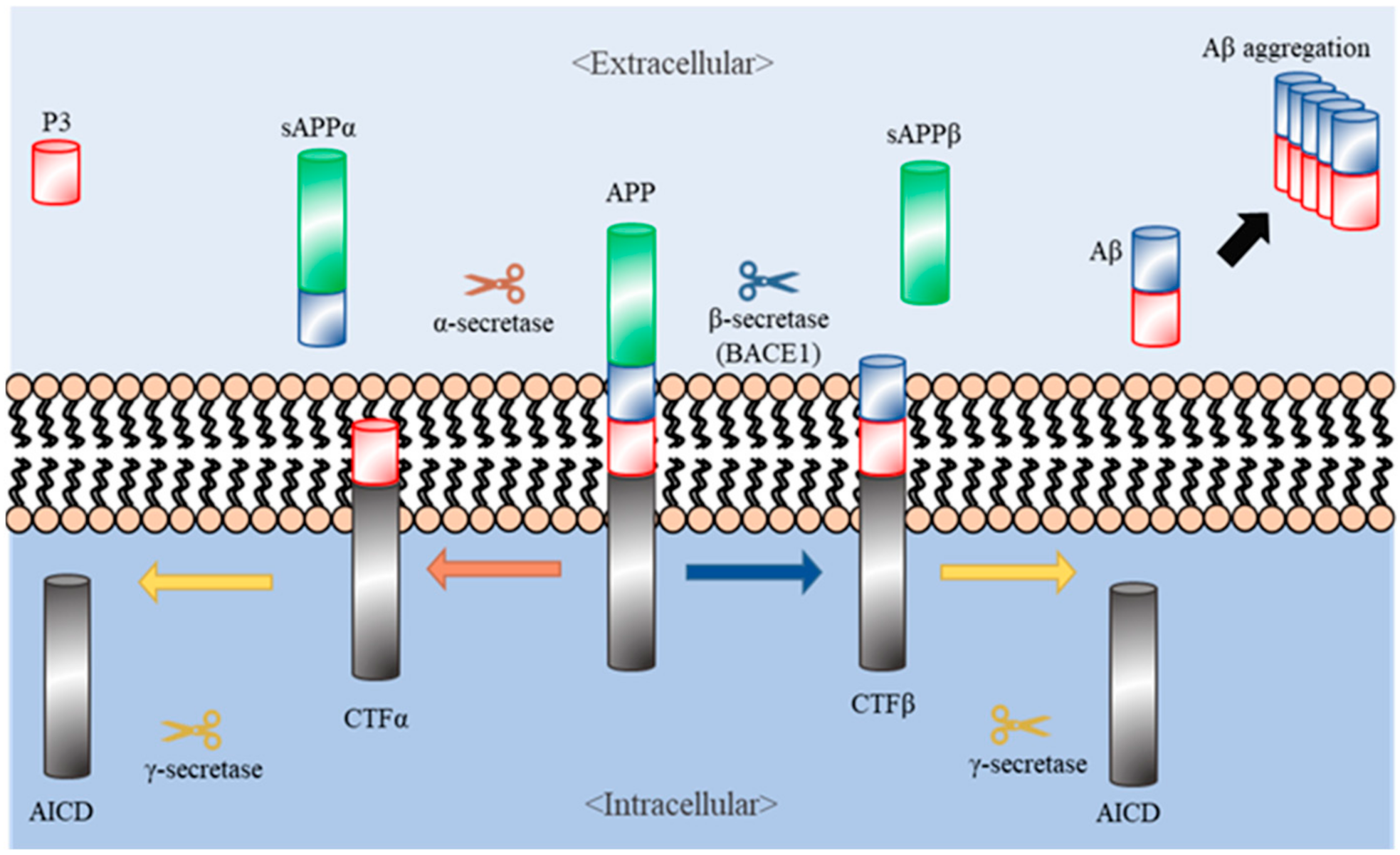
Lee, J.-H., Int. J. Mol. Sci.2021, 22, 2341.
ApoE ε4의 down-regulation을 통한 알츠하이머 치료
듀크 대학교 의과대학에서는 크리스퍼를 이용하여 ApoE ε4 유전자의 발현을 낮추기 위한 작업을 진행하고 있습니다.
ApoE는 지방 운반 물질로서 신경계의 손상 후 지방대사를 조절하는 역할로 알려져있고, ε2, ε3, ε4의 유형이 있어 ε4를 가지고 있으면 치매의 위험인자로 알려져 있습니다.
- ApoE ε4만 2개를 가지고 있는 경우는 전체 인구의 5%에 불과합니다.
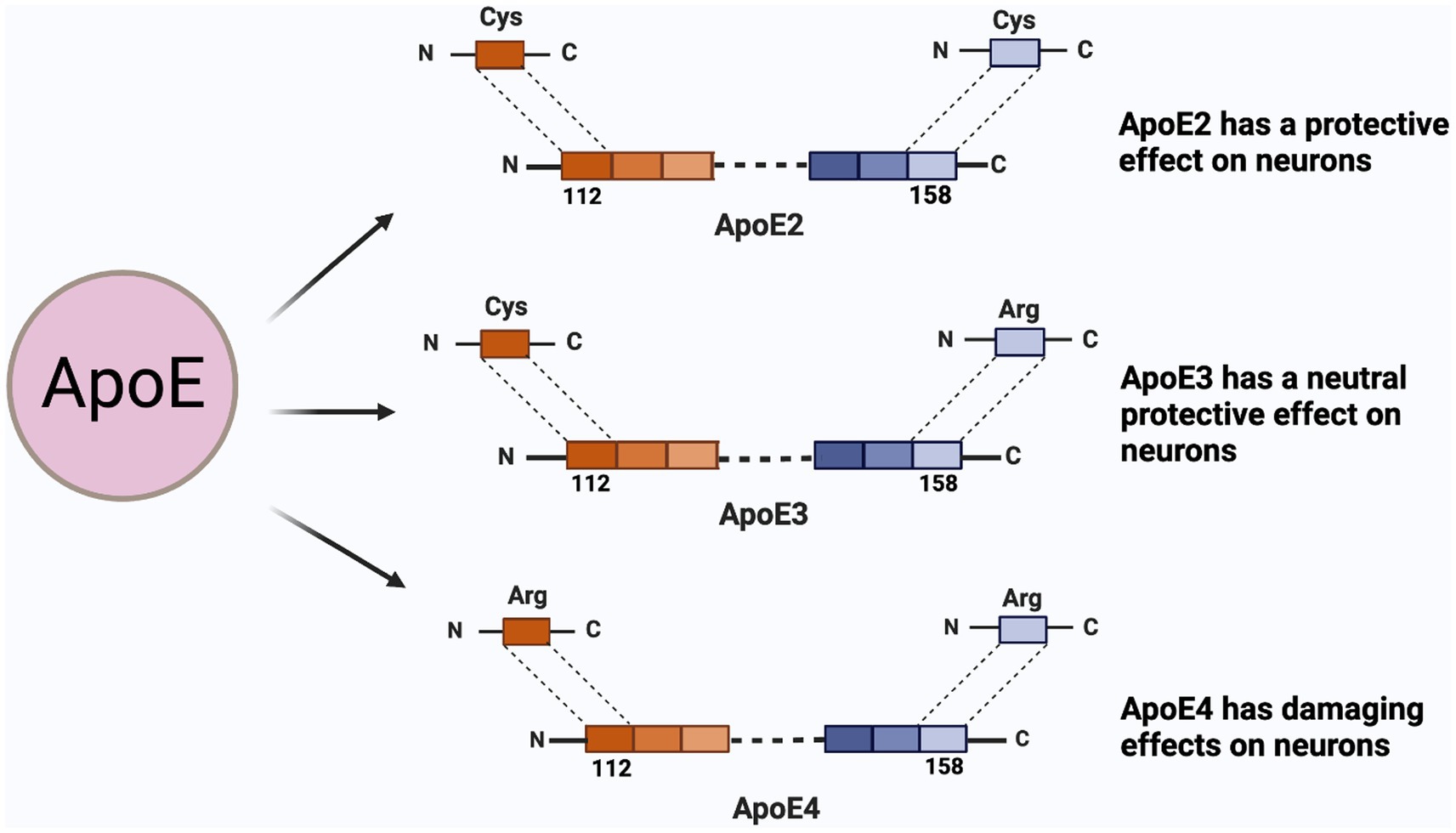
Zhang L, Aging Neurosci. 15:1199434.
연구팀은 크리스퍼의 정교한 편집기술을 통해 ε2, ε3는 건드리지 않고 ε4만 건드리는 것을 목표로 하고 있습니다.
이들은 알츠하이머 환자의 인간 유도 만능 줄기세포(hiPSC)에서 추출한 미니어처 뇌, 그리고 인간화 마우스 모델에서 ApoE ε4 발현을 낮추는데 성공했습니다.
- 또한 가장 흔한 변이인 ε3 유전자의 편집 징후는 발견되지 않았습니다. 따라서 ε4와 ε3를 하나씩 가지고 있는 경우라도 해당 크리스퍼 기술을 사용하기 안전하다고 판단하고 있습니다.
연구팀은 이를 토대로 CLAIRIgene이라는 회사를 설립, IND를 위한 ADME/T 및 PK/PD/tox study를 준비하고 있다고 밝히기도 했습니다.
동물에서 사람으로 넘어가기 위한 관문 (중개연구의 중요성)
하지만 이와 같은 결과에도 아직 걱정을 가진 연구진들은 많습니다.
결국 중요한 건 동물실험이 인체실험으로 가기에 충분한 근거를 마련했냐는 것이죠.
제일 먼저 제기되는 문제점은 크리스퍼의 전달체로 쓰이는 AAV에 대한 면역원성(immunogenicity)입니다. AAV 자체가 자연에 존재하는 바이러스인 만큼, 전달 전에 파괴될 가능성이 높죠. 이는 외부 단백질로 인식되는 CRISPR역시 마찬가지 입니다.
또한 전달력 자체에 대한 문제점도 제기됩니다. 크리스퍼를 통한 치료제가 모든 뇌세포에 효과적으로 전달되기는 어렵고, 약 수 퍼센트(%)만이 전달될 것으로 현재는 보고 있습니다. 그렇다면 이 수치가 과연 알츠하이머를 치료하는데 충분한 양인지 문제가 남게됩니다. CNS에 작용해야 하는만큼 이러한 문제는 해결이 더욱 어렵죠.
이 외에도 표적 물질에 대한 주의 의견도 있습니다.
앞서 언급된 APP는 시냅스를 안정화시키고 통합하는 등 여러 역할을 하기 때문에, 이를 편집하는 것은 굉장히 위험할 수 있습니다.
또한 amyloid-β (Aβ) domain이 변경되는 경우, infection에 취약해지고 시냅스가 꺼지지 않고 발화될 것으로 보는 의견도 존재합니다.
위험성이 큰 만큼, ApoE ε4 치료제의 경우는 ε4 선택성과 무관하게, ε4가 2개 모두 있어서 위험이 큰 사람을 대상으로만 치료제를 써야한다고 주장하기도 합니다.
결국 크리스퍼에 대해 잘 모르는 상태에서 임상시험을 시작하면, 그 피해는 결국 환자들이 입게될 것이라는 경고로 볼 수 있겠습니다.
본 글은 아래 기사를 토대로 편집/재가공하여 발행되었습니다.
CRISPR Shows Preclinical Promise in Treating Alzheimer’s, Challenges Persist, Biospace







![[임상 중단] 다케다와 드날리, 공동개발중이던 알츠하이머 치료제 연구 종료의 썸네일 이미지](https://cdn.maily.so/202308/bioglobe/1691625871601719.jpg)