2001년부터 20년 넘게 3상을 시도했지만 이제서야 성공을 한 약물이 있습니다. 바로 노바티스의 아트라센탄(atrasentan)입니다.
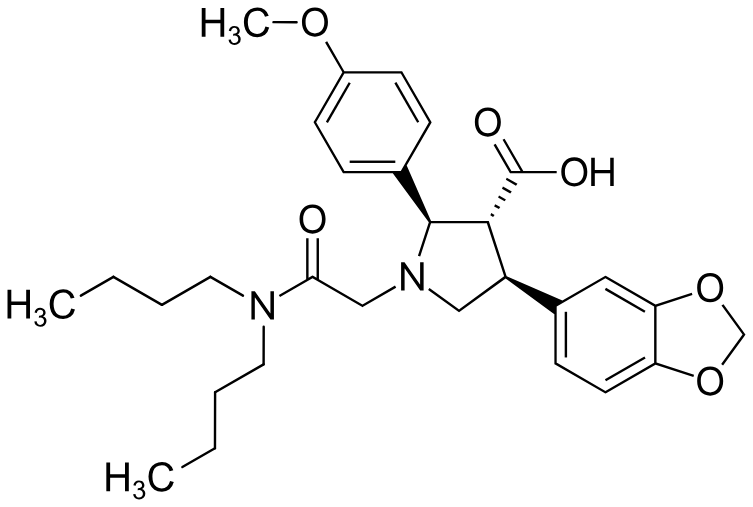
지난 20여년 동안 약물은 변화가 없었고, 오로지 임상 디자인과 적응증의 변화만 있었을 뿐이죠.
당시 같이 개발되던 약물들은 이미 특허까지 만료된 경우가 대부분인데, 이 약은 어쩌다 이제서야 승인을 받게 되었을까요?

Atrasentan, 항암제로의 시작
아트라센탄은 원래 애보트에 의해 개발된 약입니다.
애브비의 분사가 2013년이니, 그 전까지는 애보트의 소유였습니다.

Endothelin A receptor라는 혈관수축/팽창에 관여하는 물질의 길항제로 90년대에 이미 개발되었고,
당시에는 ETAR antagonist가 전립선암에 효과가 있을것이라는 가설이 있었기에 3상 임상을 진행했었습니다. ('01~'03)
그러나 2개의 3상은 실패로 끝났고, 회사는 그럼에도 어정쩡한 데이터로 FDA에 제출을 시도했으나 자문위의 만장일치로 거절당하게 됩니다. ('05)
- 당시에는 Xinlay라는 브랜드명까지 미리 준비했었다고 하네요.
그래서인지 회사는 전립선암에 대한 미련을 놓지 못하고, 이번에는 뼈 전이가 발생한 전립선암 환자를 대상으로 적응증을 변경해봅니다. 그러나 결과는 똑같이 실패로 돌아옵니다. ('08~'10)
- 심지어 NSCLC 등의 다른 암종도 도전했으나 실패했습니다.
신증(nephropathy)으로의 전환
이쯤 되면 포기할 법도 한데, 애보트는 아직 희망의 끈을 놓지 않았습니다.
처음 개발할 당시 고혈압 치료제로도 가능성이 열려있었는데, 이때의 기억을 되살려 순환계와 연관을 지어보기로 하죠.
마침 ETAR 길항제에 대한 연구가 활발히 진행되면서 혈압강하 외에도 단백뇨 및 신장기능 개선에 효과가 있을 수 있다는 결과가 나오기 시작합니다. ('11)
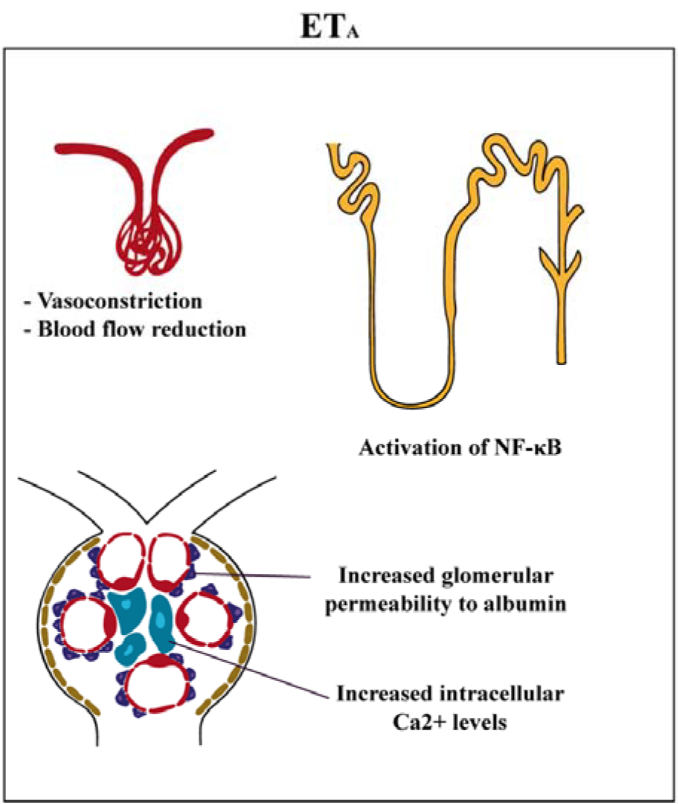
이에 애보트도 적응증을 변경, 신증에 집중하기로 합니다 ('11).
그리고, 애보트(애브비)가 벼르던 대규모 3상 스터디, SONAR가 진행됩니다.
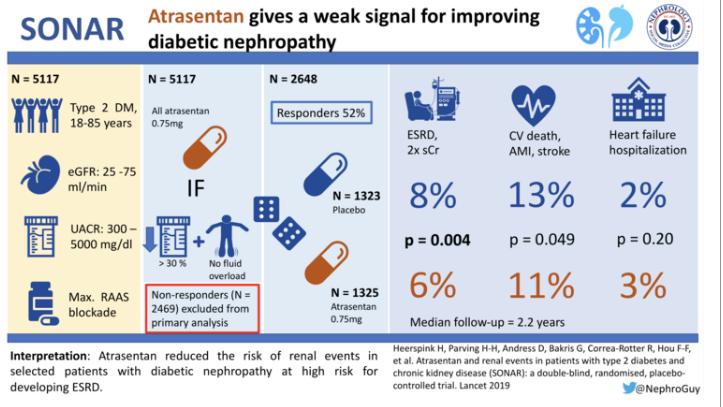
SONAR는 아트레센탄을 당뇨병성 신증에 효과가 있는지 점검한 임상시험으로, 처음에 예상한 4천명을 넘어 5600명에 달하는 환자를 모집하여 아트레센탄의 효과를 확인해봅니다. ('13~'17)
그런데 5년만의 임상치고는 결과가 애매했습니다. 결국 당뇨 환자들에게 있어 신증을 확실히 줄여준다는 임상적 증거가 부분적으로 나왔습니다.
- 물론 단백뇨의 감소는 확실히 확인했습니다.
IgA 신증(nephropathy)으로의 전략적 수정과 치누크의 매각
수년에 걸쳐 신증으로 다시 전환을 했으나, 여전히 애매한 영역에 놓여있던 아트레센탄에 구세주가 나타납니다.
바로 캐나다의 Chinook(치누크). "SONAR 데이터를 토대로 다른 희귀 사구체질환을 표적하겠다"는 목적으로 아트레센탄을 사가게 됩니다. 계약규모는 비공개. ('19)
치누크는 사구체 신장질환만을 목표로 하겠다는 목표를 세우고, 적응증을 다시 세분화합니다. 바로 희귀질환인 IgA 신증으로 바꾼것이죠.
- 아두로를 인수하여 또다른 IgA 신증 후보물질까지도 확보합니다. (zigakibart, APRIL inhibitor)
1차 평가변수 역시 임상적 지표보다는 사구체여과율(eGFR)로 확정하고, 희귀질환의 특성을 살려 임상을 진행하게됩니다.
- 20여년동안 닳고 닳은 약이라, 추가 1-2상은 불필요했고, 3상만 확실하게 하면 되는 상황이라고 판단했던 것으로 보입니다.
이런 치누크의 접근법이 마음에 들었나봅니다.
아직 3상이 채 끝나기도 전에, 노바티스가 치누크를 무려 4조원에 인수를 하게됩니다.

결국 20여년동안 애매한 성공/실패를 반복하던 아트라센탄에게 확실한 3상 성공을 처음으로 가져다주게 됩니다.
사구체여과율이 확실히 개선된 것이 확인되었습니다.
교훈
20년 가까이 고생하던 약에게 적절한 적응증과 평가지표를 찾아준 벤처는 4조원에 회사를 매각하는데 성공했습니다.
노바티스는 4조원을 지불한 가치를 충분히 보상받을 예정입니다. IgA 신증 시장을 큰 규모로 독점할 수 있을것으로 보이기 때문입니다.
- C3b를 표적하는 자체개발 치료제인 입타코판과,
- ETAR의 antagonist인 아트라센탄이 모두 3상에 성공했고,
- APRIL inhibitor인 지가키바르트도 1/2상이 긍정적인 상황입니다.
아스트라제네카가 알렉시온을 통해 희귀질환 하나로 어마어마한 수익을 낸 것 처럼, 노바티스도 비슷한 전략을 취할 수 있게 되었습니다.
이러한 사례를 통해, 신약 개발을 처음부터 끝까지 끌고가는 시대는 끝났다는 점을 다시금 확인할 수 있습니다.
또한 약이 좋다고 해서 반드시 허가를 받을 수 있는 것도 아니기에, 꼼꼼한 데이터 해석과 정교한 임상디자인, 잘 짜여진 허가전략이 엮여야 할 것 같습니다.
치누크가 노바티스에 매각되기 위해 어떤 포지션을 취했는지, 당시의 경쟁상황 등이 궁금하신 분들은 링크드인으로 연락주시면 상세히 설명드릴 수 있도록 하겠습니다 :)