국내 기업이 개발한 항암제가 올해 8월 미국 FDA 승인을 받았습니다.
그 주인공은 바로 lazertinib(레이저티닙)인데요, 우리나라에서는 이미 2021년 렉라자라는 상품명으로 출시된 약입니다. 국내 기업인 오스코텍과 그 자회사인 제노스코가 개발하였고, 전임상 단계에서 유한양행에 기술 이전을 했어요.
2018년 유한양행은 이 약물의 글로벌 개발 및 상업화 권리를 J&J의 자회사인 얀센(Jassen)에 기술 수출했어요. 무려 1조 6000억 규모의 빅 딜이었죠.

Lazertinib은 2024년 8월 19일, 비소세포폐암의 1차 치료제로 FDA 승인을 받았어요. 다만 여러가지 조건을 충족해야 되는데요, 자세한 내용은 뒤에서 얘기할게요.
Lazertinib(레이저티닙)의 한국 이름은 '렉라자', 미국 이름은 '라즈클루즈(Lazcluze)'입니다. 지금부터는 lazertinib으로 통일해서 작성할게요.
💡Lazertinib은 어디에 쓰이는 약인가요?
(FDA 허가사항 기준으로 말씀드립니다.)
Lazertinib은 국소 진행성 또는 전이성 비소세포폐암 환자의 1차 치료로 허가되었어요.
- 국소 진행성(locally advanced) 폐암: 암세포가 폐를 벗어나지 않았지만, 주변 조직이나 림프절까지 퍼져 더 이상 수술로 완전히 제거하기 어려운 상태
- 전이성(metastatic) 폐암: 암세포가 폐를 넘어 다른 장기(뇌, 간, 뼈 등)로 퍼진 상태
다만 여기에는 몇 가지 조건이 붙어요.
- Lazertinib 단독으로 사용하지 않고, amivantamab(아미반타맙)이라는 항암제와 함께 사용해야 돼요. Amivantamab 역시 비소세포폐암 치료제로, Rybrevant(리브리반트)라는 상품명을 가지고 있어요.
- EGFR이라는 특정 단백질에 돌연변이가 있어야 해요. Exon 19 결손 또는 exon 21 L858R 치환 변이가 있는 환자들을 대상으로 한 약이에요.

너무 복잡하죠? 이해하기 쉽게 추가 설명을 준비했어요.
Q. 비소세포페암이란?
폐암은 암세포의 크기, 형태 등 조직학적 특징에 따라 소세포폐암과 비소세포폐암으로 분류해요. 비소세포폐암(non-small cell lung cancer, NSCLC)은 전체 폐암 환자의 약 85%를 차지합니다.
Q. 비소세포폐암에서 EGFR 돌연변이가 왜 중요한가요?
먼저 EGFR이란, 세포 성장과 분열을 조절하는 중요한 단백질이에요. 세포가 자라거나 분열할 때 필요한 신호를 보내는 역할을 하죠.
그런데 특정 돌연변이가 생기면, EGFR이 계속 활성화되어 암세포가 멈추지 않고 자라게 됩니다. EGFR 돌연변이는 비소세포폐암 환자의 약 10~15%에서 발견되며, 특히 아시아인에서 발생 빈도가 높아요.
대표적인 EGFR 돌연변이로 exon 19 결손 또는 exon 21 L858R 치환 변이가 있어요.
- Exon 19 결손: EGFR 유전자의 19번 엑손에서 염기 서열이 삭제되어 EGFR 단백질의 과도한 활성화를 유발하는 변이입니다.
- Exon 21 L858R 치환: EGFR 유전자의 21번 엑손에서 류신(Leucine)이 아르기닌(Arginine)으로 바뀌어 EGFR 단백질이 지속적으로 활성화되는 변이입니다.
💡Lazertinib의 작용기전이 궁금해요.
Lazertinib은 암세포의 변이가 있는 EGFR*에 달라붙어서, 해당 EGFR의 작용을 비가역적으로 억제해요. 그러면 암세포는 계속 자라는 데 필요한 신호를 받지 못해 더 이상 성장하지 못하고 죽게 됩니다.
*exon 19 결손 또는 exon 21 L858R 치환 변이
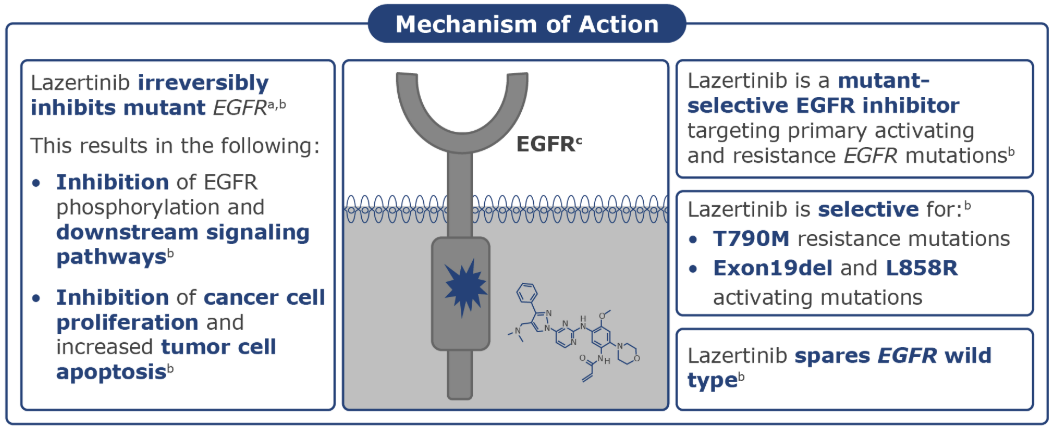
더 자세히 말하자면, Lazertinib은 EGFR을 타겟하는 TKI(Tyrosine Kinase Inhibitor)입니다. Tyrosine kinase는 세포 내에서 단백질에 인산기를 붙이는 효소인데, 세포의 성장과 생존에 중요한 신호전달에 관여해요. EGFR은 세포 표면에 있는 수용체로, 신호를 받으면 내부의 tyrosine kinase를 활성화시킴으로써 세포 성장과 생존을 돕는 단백질입니다.
Lazertinib은 EGFR의 tyrosine kinase 활성을 억제해 암세포의 성장 신호를 차단하는 표적 항암제예요. 정상 세포의 EGFR 보다 돌연변이가 있는 EGFR를 선택적으로 억제하도록 설계되었어요.
Q. Lazertinib은 amivantamab과 병용하는 조건으로 승인되었는데, 둘의 차이는 무엇인가요?
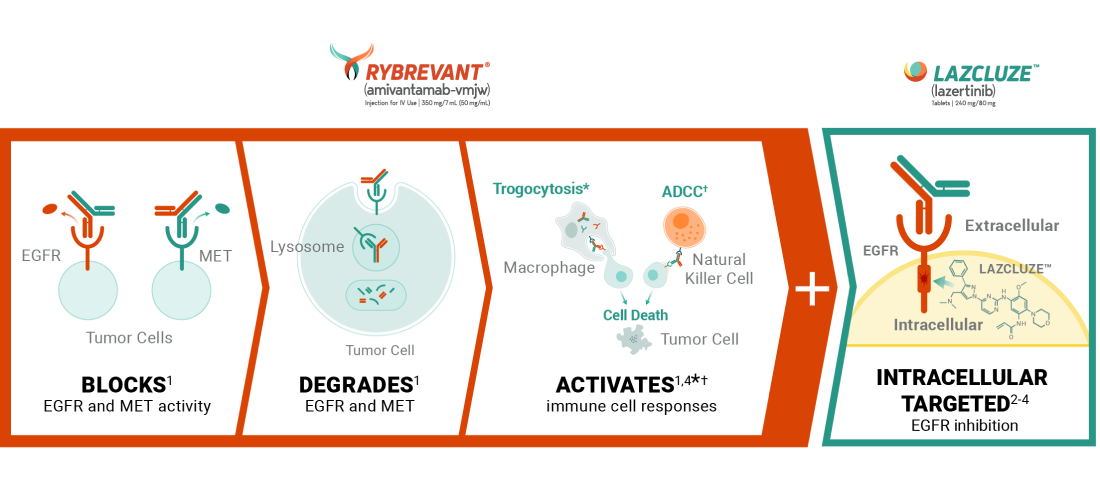
Lazertinib은 돌연변이가 있는 EGFR만을 억제하는 TKI인 반면, Amivantamab는 Y자 모양의 항체 단백질로 두 가지 방법으로 작용해요:
- 암세포 표면의 EGFR과 MET을 동시에 막아 암세포의 증식을 억제해요. MET는 EGFR처럼 암세포의 성장과 생존을 돕는 단백질이에요.
- NK세포 같은 면역세포에게 "여기 암세포가 있어요!!"라고 알려주는 길잡이 역할을 해요. 이를 통해 면역세포가 암세포를 찾아가 공격하는 ADCC(항체 의존성 세포독성) 반응을 일으킵니다.
💡Lazertinib의 임상 시험 결과가 궁금해요.
Q. 연구는 어떤 방식으로 진행되었나요?
Lazertinib의 FDA 승인에 핵심적인 역할을 한 건 MARIPOSA 연구예요.
MARIPOSA 연구는 EGFR 돌연변이(exon 19 결손 또는 exon 21 L858R 치환)가 있는 국소 진행성/전이성 비소세포폐암 환자 중 이전에 치료 경험이 없는 환자들을 대상으로 진행된 다기관, 무작위, 3상 임상시험이에요.

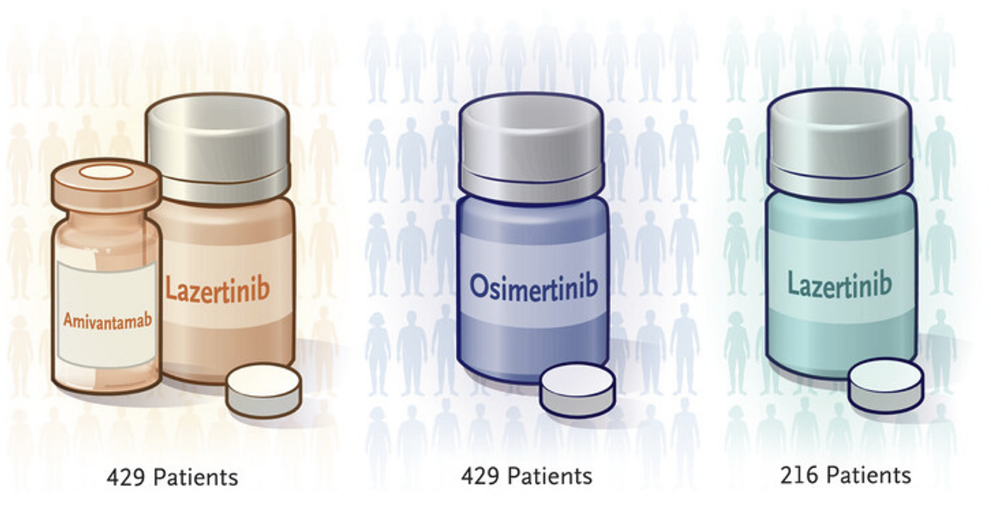
총 1074명의 환자를 세 군으로 나눴어요. (2:2:1 비율)
- Lazertinib + Amivantamab 병용군 (429명, open-label)
- Osimertinib 단독군 (429명, double-blind)
- Lazertinib 단독군 (216명, double-blind)
*Open-label과 Double-blind의 차이가 궁금하다면 지난 뉴스레터를 참고해주세요.
Osimertinib(오시머티닙, 상품명: Tagrisso/타그리소)은 EGFR 돌연변이 비소세포폐암의 표준치료제(1차 치료제)예요. 3세대 EGFR-TKI로 효과가 우수해서, 새로운 치료법인 Lazertinib + Amivantamab 병용요법의 효과를 평가하기 위한 비교 대상으로 선택되었어요.
Q. Primary end point는 무엇이었나요?
임상시험의 primary end point(일차평가변수)는 그 치료법의 효과를 판단하는 가장 중요한 기준이에요.
MARIPOSA 연구의 primary end point는 눈가림 독립중앙검토(BICR)를 통한 무진행 생존기간(PFS)이었어요. BICR은 임상시험 결과의 객관성을 높이기 위해 환자가 어떤 치료를 받았는지 모르는 상태에서 독립적인 전문가들이 평가하는 방식이에요.
무진행 생존기간(progression-free survival, 이하 PFS)이란, 약물 투여를 시작한 이후 질병이 진행되거나 환자가 사망할 때까지의 기간을 의미해요. PFS가 길수록 그 치료법이 암의 진행을 잘 막아준다는 뜻입니다.
Q. 두 그룹의 PFS 결과는 어땠나요?
아래 표를 보면 알 수 있어요. PFS에 관한 내용을 하나씩 해석해볼게요.
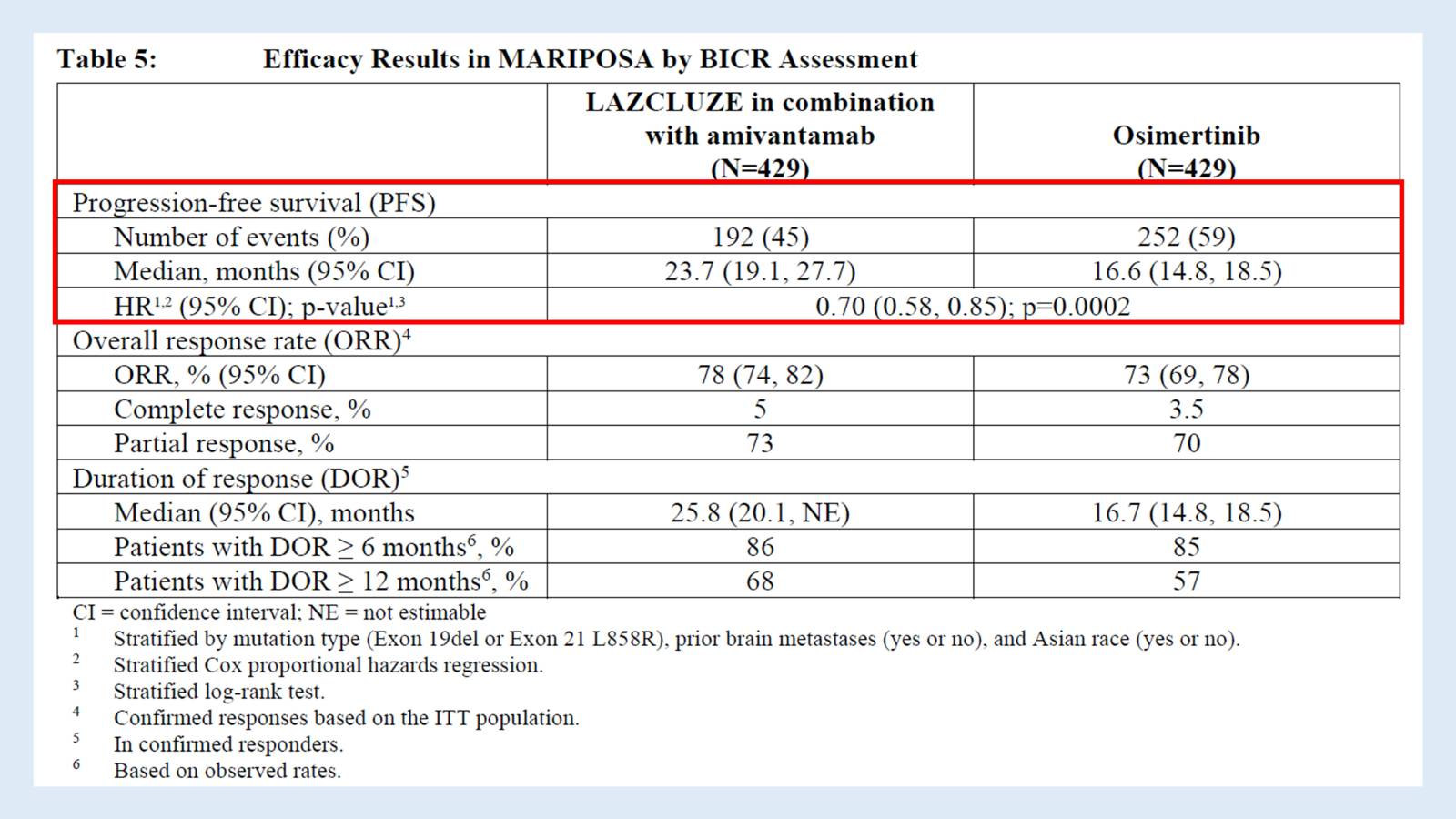
Number of events (%)
여기서 ‘이벤트(event)’는 '질병 진행(progression)' 또는 '사망(death)' 중 하나가 발생한 경우에요. 즉, 치료 후 일정 기간 동안 암이 악화되거나 사망한 환자 수를 의미합니다.
Lazertinib + Amivantamab 병용군
: 질병 진행이나 사망이 발생한 환자 192명 (전체의 약 45%)
Osimertinib 단독군
: 질병 진행이나 사망이 발생한 환자 252명 (전체의 약 59%)
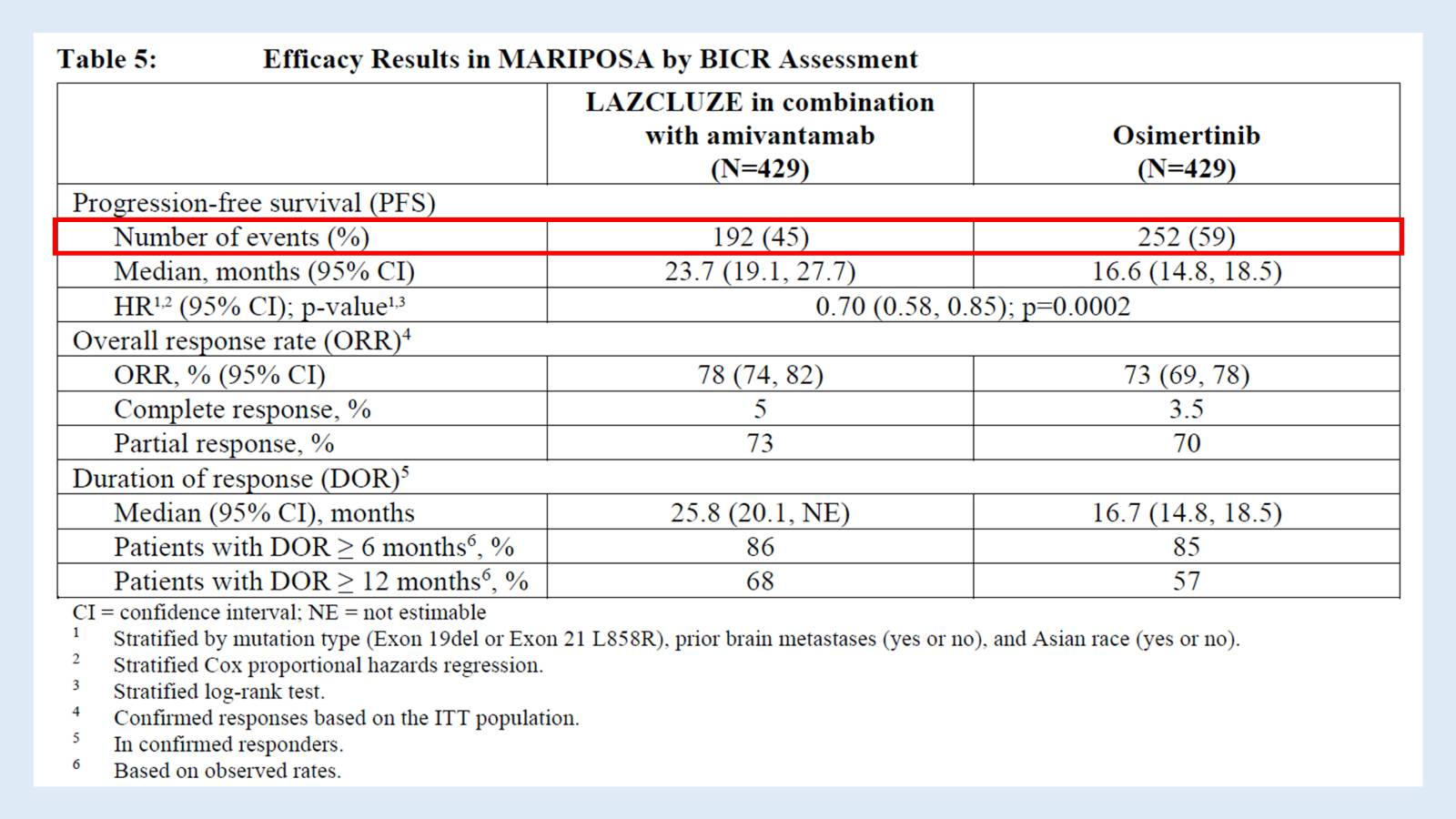
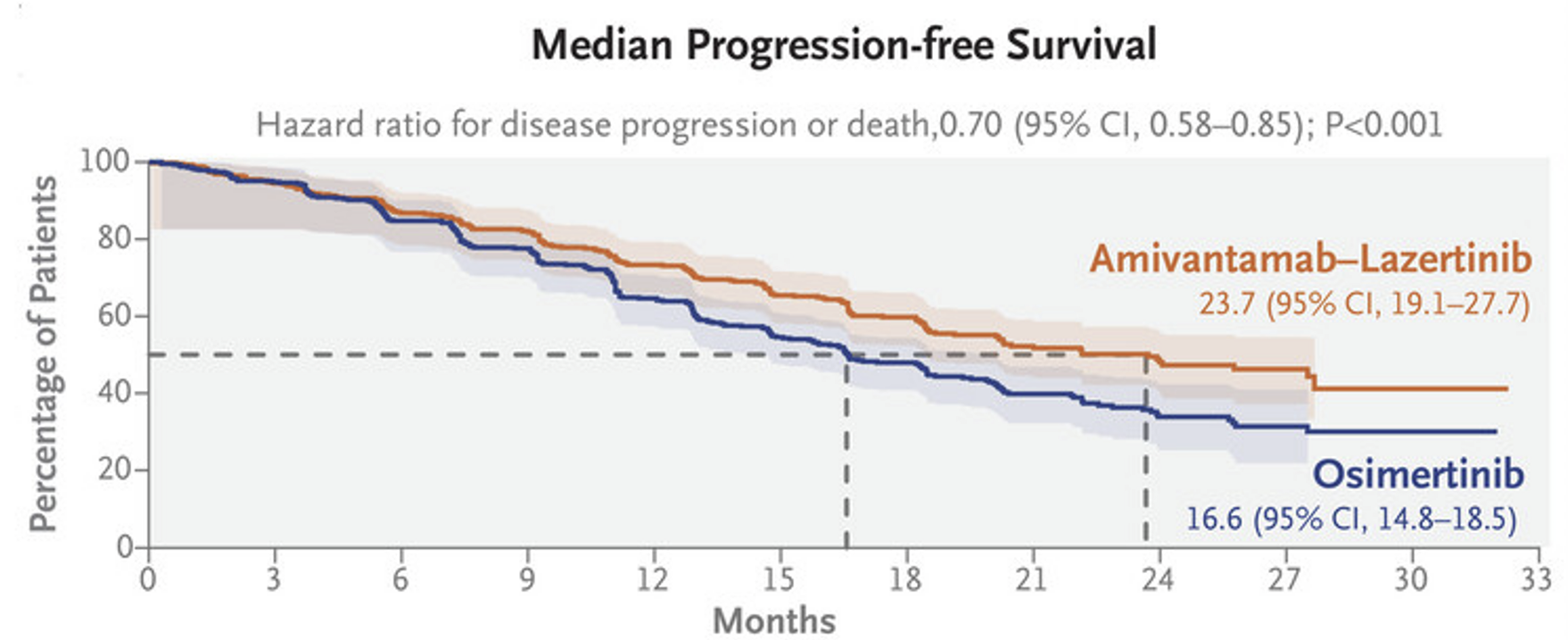
Median PFS (단위: months)
Lazertinib + Amivantamab 병용군: 23.7개월 (95% CI: 19.1~27.7개월)
Osimertinib 단독군: 16.6개월 (95% CI: 14.8~18.5개월)
Lazertinib + Amivantamab 병용군이 Osimertinib 단독군에 비해 PFS 중앙값이 약 7개월 정도 더 길었어요. 즉, 암이 진행되지 않고 지낸 기간이 평균적으로 7개월 더 길었다는 뜻이죠.
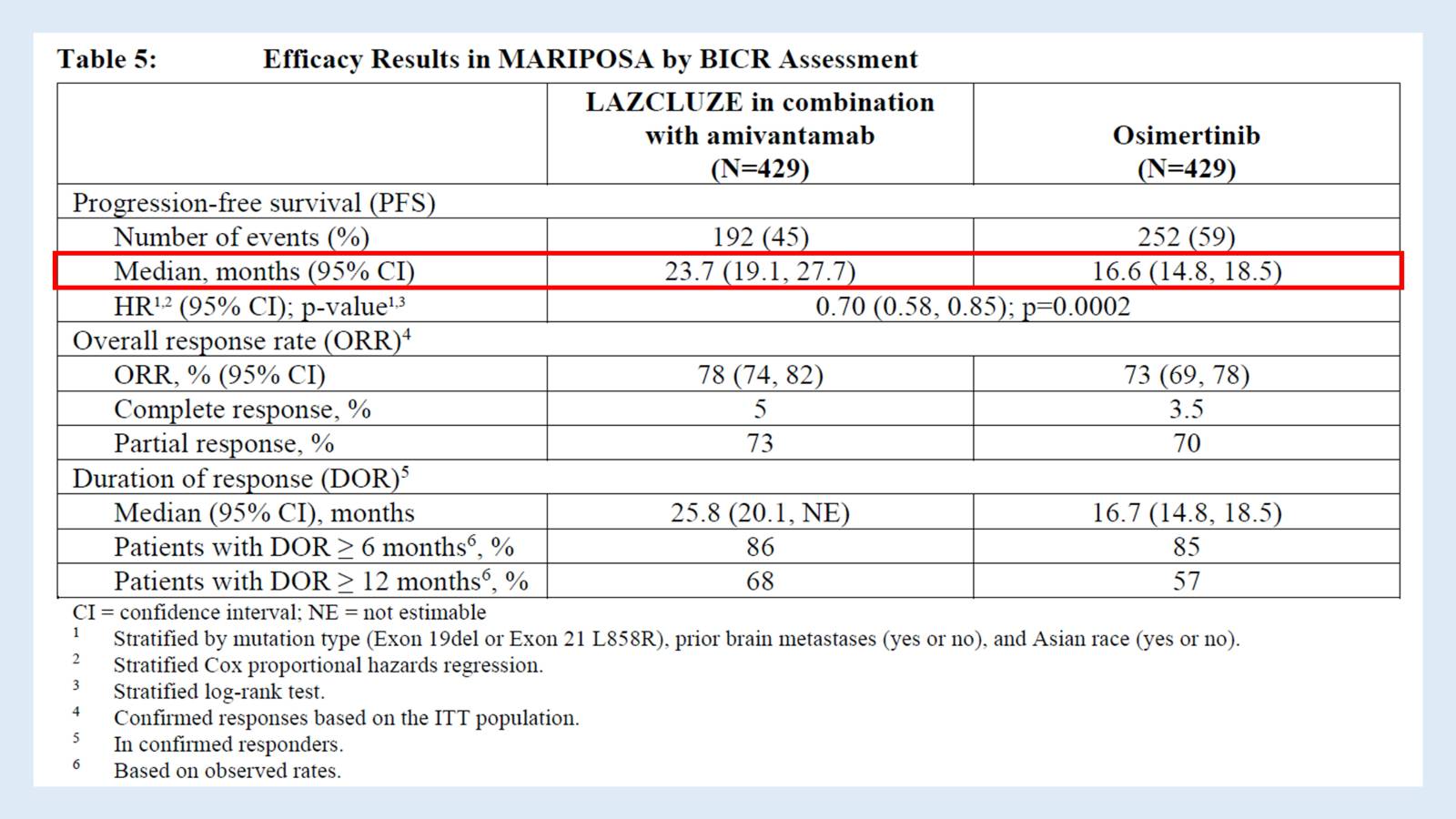
HR = 0.70, p = 0.0002의 해석
HR(hazard ratio, 위험비)은 생존과 관련된 위험을 정량화하는 방법이에요. 생존 분석(survival analysis)에서 흔히 사용되는데요, 생존 분석이란 특정 사건의 발생까지 걸리는 "시간"을 통계적으로 다루는 분석 기법을 말해요.
HR은 생존 분석에서 두 집단 간 특정 이벤트(ex. 질병 진행, 사망)가 발생하는 위험률의 비율을 의미해요:
HR = (실험군의 위험률) / (대조군의 위험률)
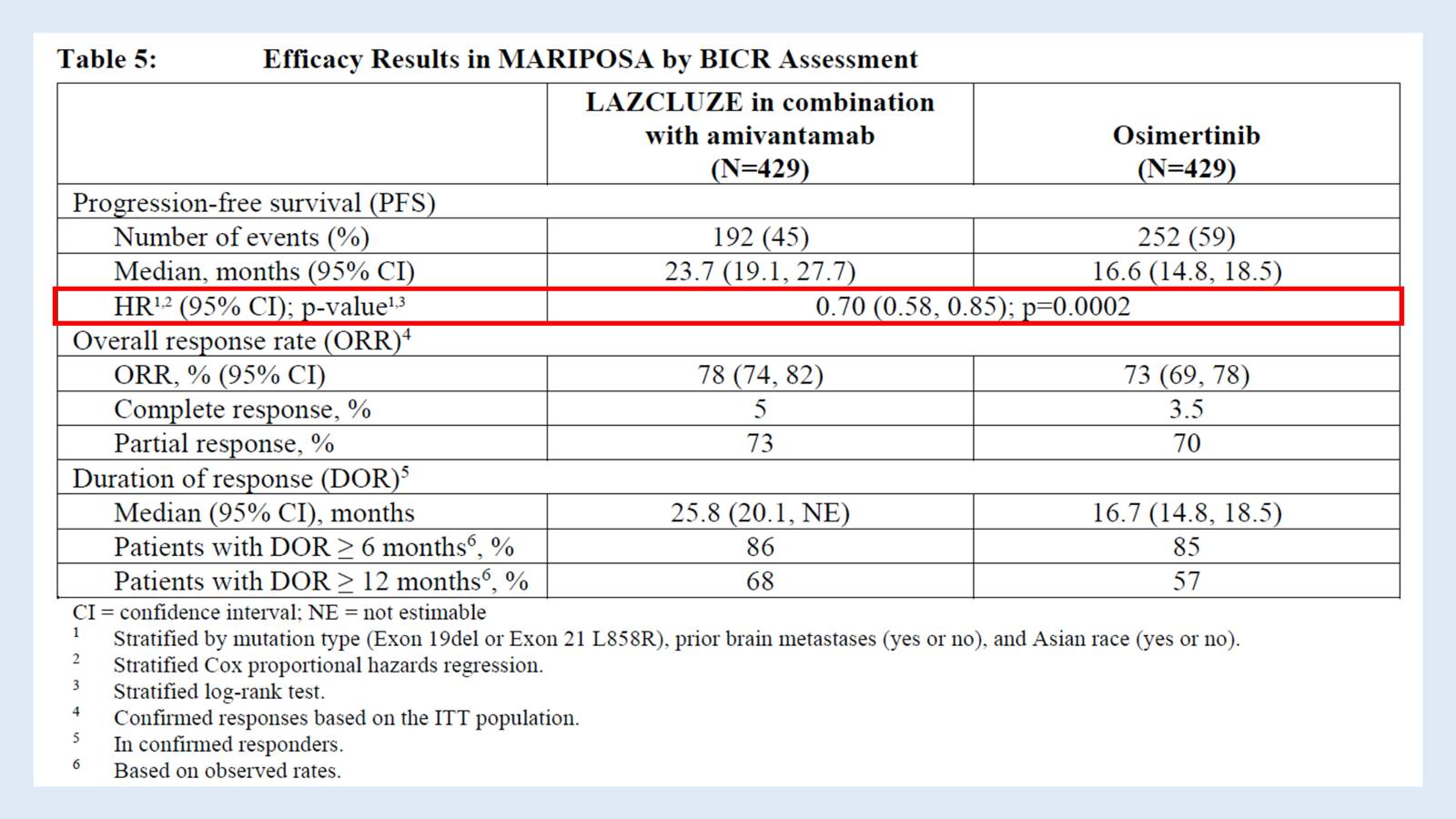
위험비(HR)가 1보다 작으면 실험군이 대조군에 비해 질병 진행 또는 사망 위험이 낮다는 뜻이에요.
위의 표에서 HR = 0.70은 이렇게 해석할 수 있어요:
Lazertinib + Amivantamab 병용요법은 Osimertinib 단독요법에 비해 암이 진행되거나 환자가 사망할 위험이 30% 더 낮았다.
또한 p값이 0.0002라는 것은 통계적으로 매우 유의한 차이가 있음을 말해요. 이런 결과가 우연히 나타날 확률이 매우 낮다는 뜻입니다.
* p-value에 대한 자세한 설명은 지난 뉴스레터를 참고해주세요.
Q. PFS를 Kaplan-Meier Curve로 표현한다면?
카플란-마이어 곡선(Kaplan-Meier curve)은 생존 분석에서 시간 경과에 따른 생존 확률(또는 이벤트 없이 유지되는 비율)을 추정해 그래프로 나타낸 것입니다. 생존 데이터를 표현하는 가장 일반적인 방법이에요.
생존률 100%에서 시작해서 점점 감소하는 형태를 보여요.
같은 그래프이지만 Number at risk가 함께 표시된 버전도 가져왔어요.
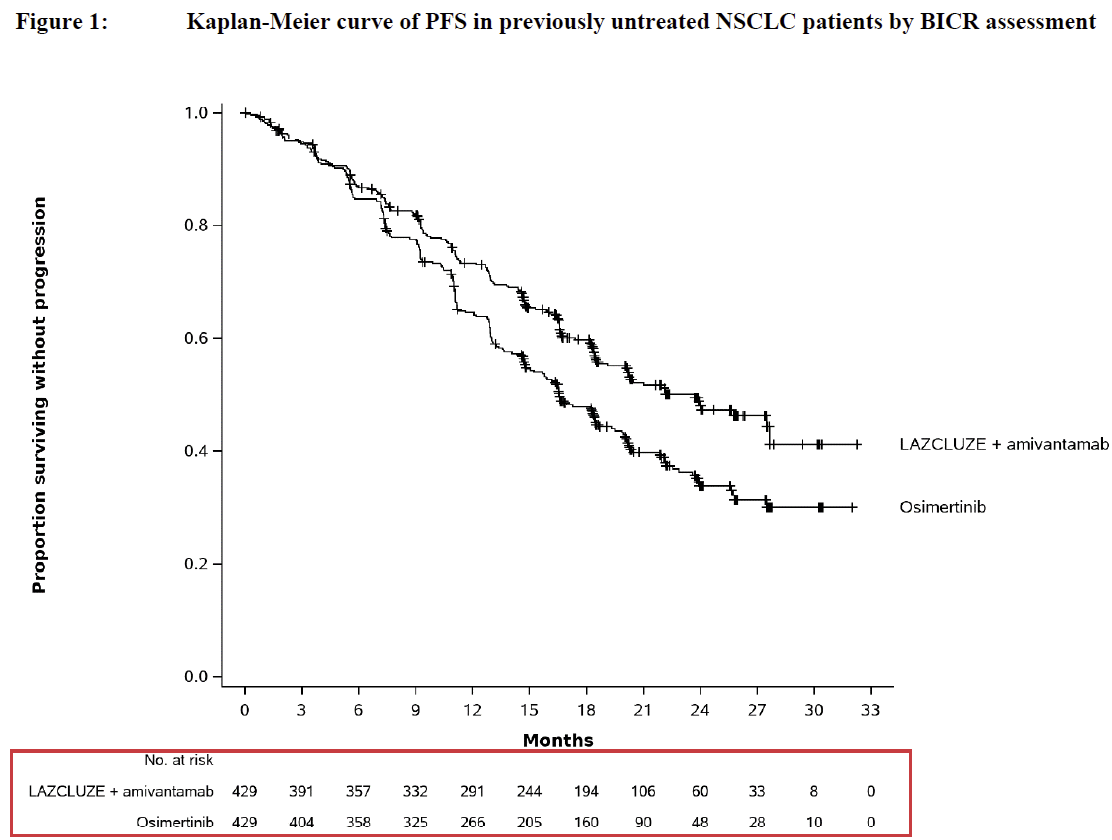
Number at risk는 특정 시점에서 이벤트(ex. 사망, 질병 진행)를 경험하지 않았고, 추적 관찰에서 제외되지 않아 여전히 해당 이벤트가 발생할 가능성이 있는(즉, '위험 상태에 놓인') 환자 수를 의미해요.
다시 말해, 이벤트가 이미 발생한 환자 또는 추적을 실패한 환자는 number at risk에 포함되지 않아요. 오직 그 시점까지 생존하거나 이벤트 없이 남아있어 '계속 관찰 가능한' 대상자 수만 포함됩니다.
Q. PFS 관련 결과를 요약한다면?
Lazertinib + Amivantamab 병용군은 Osimertinib 단독군 대비
- 질병이 진행되지 않고 유지된 기간이 약 7개월 더 길었습니다(median PFS: 23.7 mo vs. 16.6 mo).
- 질병이 진행되거나 사망할 위험이 약 30% 낮았으며(HR=0.70), 이 차이는 통계적으로 유의했습니다(p=0.0002).
💡오늘 내용을 정리할게요.
- Lazertinib(레이저티닙)은 EGFR 돌연변이가 있는 국소 진행성 또는 전이성 비소세포폐암 환자의 1차 치료제로, 국내에서 '렉라자'로, 미국에서는 '라즈클루즈(Lazcluze)'로 알려져 있어요.
- Lazertinib은 amivantamab와의 병용 요법으로 FDA 승인을 받았어요. 또한 EGFR 돌연변이 중에서 exon 19 결손 또는 exon 21 L858R 치환 변이된 환자만을 대상으로 해요.
- 무진행 생존기간(PFS), 위험비(HR), 카플란-마이어 곡선(Kaplan-Meier curve) 및 Number at risk에 대해 설명했어요. MARIPOSA 임상 3상시험에서 Lazertinib + Amivantamab 병용 요법은 Osimertinib 대비 무진행 생존기간(PFS)을 약 7개월 연장했으며, 질병 진행 및 사망 위험을 30% 감소시켰어요.
오늘 내용이 유익했다면 약디의 뉴스레터 구독을 부탁드려요 :)
[약토피아 인스타그램] 또는 [메디컬라이터 약디 스레드]를 팔로우 하시면, 더 많은 소식을 받아보실 수 있습니다.



의견을 남겨주세요
sbs
우리나라에서 타그리소에 대적할만한 약이 나오는걸 보다니😊 존슨앤존슨이 주도했겠지만 그래도 유한양행이 정말 큰일을 해냈네요. 이번 주도 잘봤습니다 감사합니다!
약디의 뉴스레터
저도 보면서 국내 포텐셜도 대단하다는 것을 느꼈습니다 :) 오늘도 댓글 남겨주셔서 감사드려요!!
의견을 남겨주세요