BNCT가 기존 방사선 치료와 뚜렷이 다른 점은 붕소의약품을 활용한 암 표적화(Targeting)에 있습니다. 하지만 핵심은, 암세포에 얼마나 잘 붕소를 전달할 수 있느냐는 점이죠.
이번 뉴스레터에서는 이러한 붕소의약품 개발의 역사와 진화, 그리고 앞으로 어떤 시도들이 이어질지를 함께 살펴보려 합니다!
🧪붕산 (Boric acid) - BNCT의 출발점
BNCT의 시작은 1936년 미국의 물리학자 G. 로커가 처음으로 이론을 제시하며 시작되었습니다. 이후 1950년대 미국 브룩헤이븐 국립연구소(Brookhaven National Laboratory, 이후 BNL) 및 메사츄세츠 공과대학(Massachusetts Institute of Technology)을 중심으로 본격적인 임상 적용이 시도되었죠.
이때 사용된 붕소 약물이 바로 붕산(Boric acid), 붕사(Borax), 펜타보레이트와 같은 소분자 화합물이었습니다.
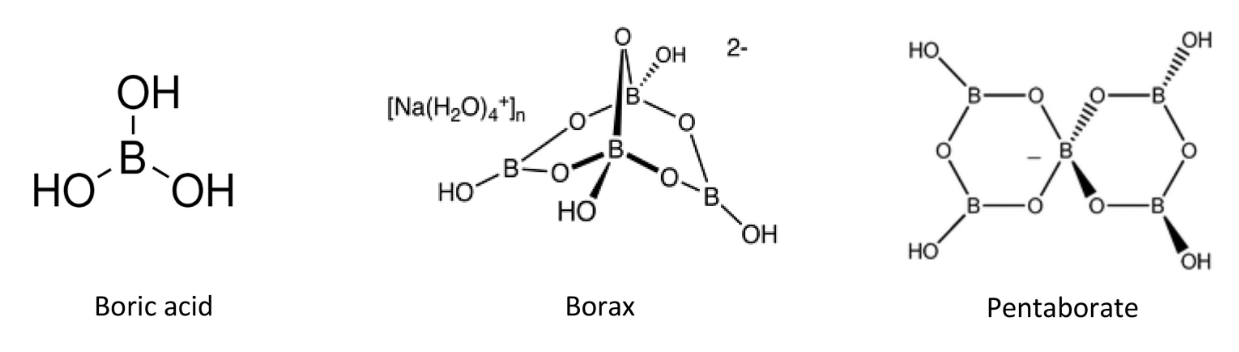
✅ 단순한 구조와 높은 수용성
이러한 초기 붕소 약물들은 구조가 단순하고 수용성이 좋아서, 붕소를 체내에 도입하기 위한 첫 시도로서 적합했습니다. 특히 낮은 독성과 상대적으로 안전한 물질이라는 점도 초기 연구자들의 선택에 영향을 주었습니다.
⛔ 낮은 종양 특이성
하지만 모두 종양세포에 특이적으로 쌓이지 않는다는 한계가 있었습니다.
즉, 종양세포 내 충분한 농도의 붕소를 축적시키기 어려웠고, 그 결과 정상 조직과 종양 조직 간 붕소 농도 비율이 1 이하로 낮아, 정상 조직의 방사선 손상 위험을 높이는 문제도 있었습니다.
⏩ 선택적 붕소 전달 개념 발전
비록 이러한 초기 붕소 약물들이 BNCT 용 약물로는 실패하였지만, "종양 선택적 붕소 섭취"가 있어야 효과적이라는 BNCT 치료의 토대를 마련하였습니다. 이는 추후 BSH, BPA 등 더 개선된 붕소 약물의 개발로 이어지는 발판이 되었습니다.
🔬종양 선택성을 높여라 - BSH, BPA의 개발
그 이후 시도된허가된 붕소 의약품은 소듐보로캅테이트(Sodium Borocabtate)와 보로노페닐알라닌(Boronophenylalanine)이 있습니다. 각각 BSH, BPA로 불리는 화합물이죠
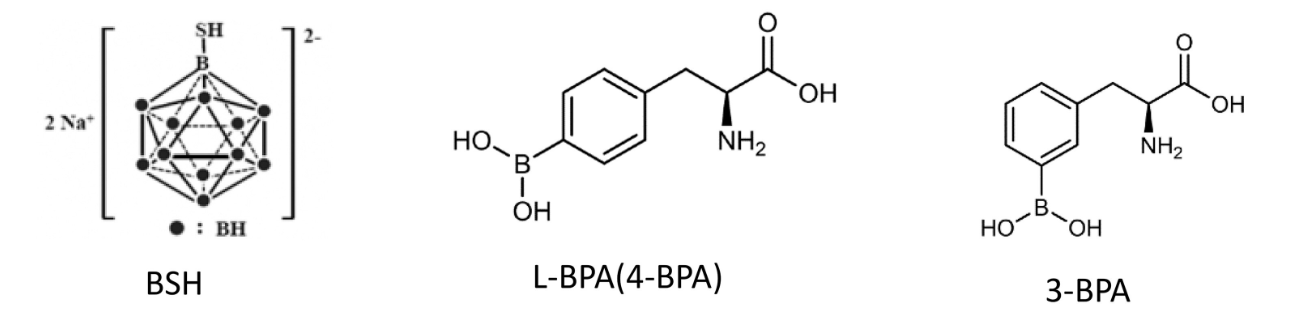
1️⃣ BSH - 고붕소 함량 붕소 전달체
BSH는 1968년 일본의 하타나카 박사의 악성 뇌종양 환자 대상 BNCT 임상시험에서 활용되기 시작하며 1970~80년대 일본과 독일에서 활발하게 연구되었습니다.
✅ 붕소 클러스터
BSH는 한 개의 분자에 12개의 붕소 원자를 담을 수 있다는 구조로 인해 주목을 받았습니다. 이론상 높은 치료 효과를 기대할 수 있었고, 구조적으로 안정적이며 수용성이 높았죠. 이로 인해 정맥주사로 쉽게 투여가 가능하다는 장점도 있었습니다.
하지만 마찬가지로 임상 적용에 큰 벽이 있었습니다.
⛔ BSH, 여전히 낮은 종양 선택성
BSH는 수동적 확산에 의존하여 조직에 분포하면서, 종양세포보다 주변 정상세포에 비슷한 농도로 축적되는 양상을 보였습니다. 특히, 종양세포 내부로 흡수되지 않고 주로 세포외액에 머무르는 특징 때문에 세포 내 핵 손상 유도가 어려웠습니다. 게다가 혈관뇌장벽(Brain-Blood Barrier, BBB)를 통과하지 못해 뇌종양에서 치료 효과가 제한적이었죠.
2️⃣ BPA - 트로이의 목마
BPA는 인체 필수 아미노산 중 하나인 페닐알라닌(Phenylalanine)의 유사체로, 대사가 활발한 종양에서 선택적 축적이 가능할 것이라고 판단되어 개발되었습니다.
✅ BPA, 우수한 종양 선택성 및 높은 세포 흡수성
종양세포는 세포 분열이 빠르기 때문에 이러한 아미노산을 흡수하는 수용체가 정상세포에 비해 훨씬 많이 발현되어 있고, BPA는 이런 수용체를 사용해서 세포 내부로 원활하게 들어가게 되죠. 결론적으로 정상세포에 비해 종양세포 내부로 다량의 붕소가 전달되고, 세포 내부에서 강력한 방사선을 발생시킬 수 있습니다.
이러한 특징으로 인해 현재까지 가장 많이 사용되는 임상용 붕소 의약품이 되었고, 일본의 Stella Pharma 社가 시판 승인을 받은 의약품이기도 합니다.
⛔ BPA의 한계점과 도전과제
하지만, BPA는 붕소 함량이 낮습니다. 한 BPA 분자 내에 여러 개의 붕소를 달아서 전달할 수 없는 문제가 있죠. 때문에 치료 시에는 고용량의 BPA를 투약받아야 합니다.
또한, 상대적으로 수용성이 좋지 않기 때문에 소변의 BPA가 결정Crystalization)을 형성하면서 혈뇨를 유발할 수 있습니다. 또한 과당 또는 만니톨을 용매로 사용하기 때문에 과당불내증 환자에게는 사용할 수 없죠.
이런 이유로 인해, 현재는 BPA를 기반으로 한 약물 최적화와 함께 나노입자 기반 전달체 도입, BPA 유도체 개발 등 다양한 후속 전략이 연구되고 있습니다.
🚀차세대 붕소 의약품
BPA는 여전히 BNCT의 표준 약물로 쓰이고 있습니다만, 고용량 붕소 전달에 대한 니즈, 암종별 아미노산 수용체 발현 편차로 인한 종양 선택성의 제한성 등으로 인해 새로운 붕소 의약품은 계속해서 개발되고 있습니다.

1️⃣ 고분자 및 나노입자 기반 붕소 약물
종양 내 축적률을 향상시키고, 체내 순환시간을 연장시키기 위해 고분자, 나노입자 붕소 약물이 개발되고 있습니다.
고분자 물질에 붕소를 결합시켜 대사 안정성과 붕소 함량을 높이거나, 리포좀, 엑소좀 혹은 실리카 나노입자 등에 붕소를 실어서 종양에 전달하려는 나노입자 기반약물 등이 대표적이죠.
이러한 약물들은 혈액 및 종양 조직에 더 오래 머물며 높은 붕소 농도를 유지시킵니다.
또한, 동위원소(isotope)을 부착하여 진단영상 촬영과 치료를 동시에 할 수 있도록 설계하기도 합니다. 이런 것을 보통 테라노스틱스(Theranostics, Therpy + Diagnostics)라고 부르며, 환자 개인이 해당 치료제에 효과가 있을지 진단하며 치료를 진행할 수 있도록 만드는 데 사용됩니다.
2️⃣ 표적 결합체 (Targeted Boron Delivery)
항체-약물 접합체(Antibody-Drug Conjugate), 혹시 들어보신 적 있나요? ADC라는 용어가 더 친숙하실 겁니다. 바로 종양에 특이적으로 작용할 수 있는 항체에 약물을 연결하여 종양세포에 정확히 약물을 전달한다는 개념입니다. 대표적으로 허셉틴(Trastuzumab)에 세포독성 약물을 결합한 엔허투(Enhertu)가 있죠.
마찬가지로, 종양 특이적인 항체에 붕소 클러스터를 결합하여 정확히 종양세포에 붕소를 전달하려는 붕소 ADC 개발이 지속되고 있습니다. 이 외에도 세포막 표적화, 핵 표적화 등 종양 세포의 생리학적 특징을 이용해 선택성을 높이려는 차세대 붕소의약품 개발이 진행되고 있습니다.
3️⃣ 아미노산 유사체 (Amino acid analogue)
최근에는 L-BPA의 단점인 낮은 수용성과 결정화 문제를 해결하기 위해 새로운 아미노산 유사체가 연구되고 있습니다.
수용성이 개선되어 당류를 용해제로 사용하지 않아도 된다면, 붕소약물의 투여 용량, 방법 및 혈뇨의 위험 등 여러 부분들이 개선될 수 있습니다.
또한, F-18 라벨링을 통해 PET 영상 촬영이 가능한 접근도 탐색중입니다. 이러한 접근방법은 종양 내 붕소 축적 정도를 실시간으로 시각화할 수 있어, BNCT의 정확한 치료계획 수립과 예후 예측에 큰 도움이 될 수 있습니다
🔜 정리하자면,
차세대 붕소 약물의 방향성은 단순한 붕소 함량 증대에서 벗어나 아래와 같은 목표를 위해 달려나가고 있습니다.
✔️ 높은 종양 섭취
✔️ 정밀 타겟팅
✔️ 치료 효율 극대화
✔️ 부작용 최소화
✔️ 진단-치료 통합(Theranostics)
다가오는 4월의 EVENT
- 한국의학물리학회 춘계학술대회 - BNCT 연구회 발표 프로그램 🗓️

오는 4월 17일, 18일 이틀간 강릉 라카이샌드파인에서 한국의학물리학회 춘계학술대회가 개최됩니다!
4월 18일, BNCT 연구회에서 붕소중성자포획치료에 대하여 발표가 진행될 예정입니다. 다원메닥스에서 BNCT의 현황과 생물학적 원리에 대해, KRISS의 김정호 박사님께서 BNCT의 중성자 스펙트럼 측정에 대한 발표를 진행해 주실 예정이오니, 많은 관심 부탁드려요!
📖BNCT Library
효과적인 BNCT를 위한 붕소의약품 개발에 대해 어떤 최신 논문들이 있을까요? 그리고, 이번 달에 새로운 뉴스는 어떤 것들이 있을까요?
(1) 붕소의약품 개발에 대한 논문
- Fithroni AB, Inoue H, Zhou S, Hakim TFN, Tada T, Suzuki M, Sakurai Y, Ishimoto M, Yamada N, Sauriasari R, Sauerwein WAG, Watanabe K, Ohtsuki T, Matsuura E. Novel Drug Delivery Particles Can Provide Dual Effects on Cancer "Theranostics" in Boron Neutron Capture Therapy. Cells. 2025 Jan 6;14(1):60. doi: 10.3390/cells14010060. PMID: 39791761; PMCID: PMC11719788.
- Barth RF, Gupta N, Kawabata S. Evaluation of sodium borocaptate (BSH) and boronophenylalanine (BPA) as boron delivery agents for neutron capture therapy (NCT) of cancer: an update and a guide for the future clinical evaluation of new boron delivery agents for NCT. Cancer Commun (Lond). 2024 Aug;44(8):893-909. doi: 10.1002/cac2.12582. Epub 2024 Jul 8. PMID: 38973634; PMCID: PMC11337926.
- Shen, S., Wang, S., Zhou, D., Wu, X., Gao, M., Wu, J., … Wang, N. (2024). A clinician’s perspective on boron neutron capture therapy: promising advances, ongoing trials, and future outlook. International Journal of Radiation Biology, 100(8), 1126–1142.
(2) BNCT에 관련된 새로운 뉴스