코로나19에 맞서 싸우는 인류의 무기는 무엇보다도 백신입니다. 그중에서도 모더나와 화이자로 대표되는 mRNA 백신 기술은 이번 사태를 맞아 처음으로 상용화된 기술이면서도 대단한 효율을 보여주고 있어서 백신 생명공학의 새 지평을 열었다고 평가받고 있지요. 심지어 우후죽순으로 나타나는 변이 바이러스마저도 안정적으로 막아내고 있습니다.
그런데 2021년 6월 16일, mRNA 백신이라고 해서 만능은 아니라는 어찌 보면 당연하면서도 한편으로는 실망스러운 소식이 도착했습니다. 독일의 mRNA 기술 전문 회사, 큐어백(CureVac)의 mRNA 백신이 임상시험 3상에서 실패했다는 뉴스인데요, 겨우 47%에 불과한 효과를 보였다고 하네요. 어째서 이만큼이나 낮은 효과가 나온 건지, 조금 자세히 살펴보겠습니다.

큐어백의 이번 mRNA 백신은 CVnCoV라는 코드명을 부여받았습니다. 임상 1~2상 결과가 2020년 11월에 나왔으니 비교적 후발주자인 셈인데요, 영하 70도를 요구하는 화이자 백신이나 영하 20도에 보관해야 하는 모더나 백신에 비해 상대적으로 높은 온도에서도 보관할 수 있는 mRNA 백신이어서 많은 기대를 모았습니다. 큐어백의 보도자료에 따르면 영상 5도, 즉 냉장고 정도의 온도에서도 3개월 간은 보관할 수 있었거든요.
똑같은 mRNA 백신인데 왜 이렇게까지 보관 온도가 차이가 나는 걸까요? mRNA의 재료가 되는 뉴클레오사이드(nucleoside)가 조금 다르기 때문입니다. 뉴클레오사이드는 RNA를 구성하는 단위 분자인데요, 말하자면 mRNA 백신이 하나의 '문장'이라고 한다면 뉴클레오사이드는 그 문장을 구성하는 '단어'가 됩니다.
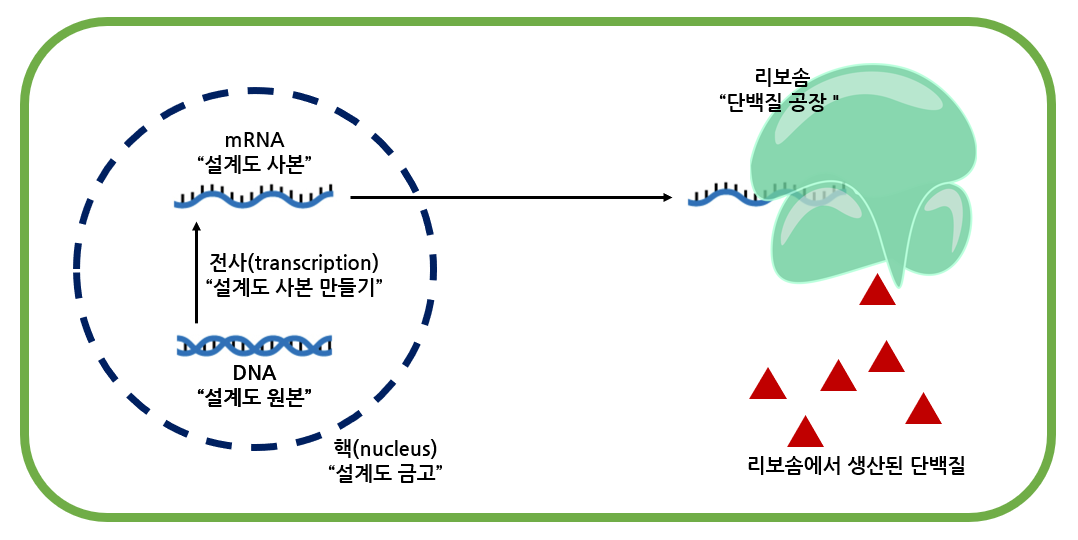
mRNA 백신의 원리를 소개한 글에서 설명드렸다시피, mRNA는 세포 내 단백질 공장에서 사용하는 레시피 사본이자, 일종의 소스 코드입니다. 프로그래밍을 공부해보신 분들이라면 인터넷에서 타인의 코드를 다운받았을 때, 혹은 동료의 코드를 전달받았을 때 갑자기 보안프로그램이 악성코드라면서 차단해 버렸던 경험이 한 번쯤은 있으실 거예요. 게시자가 불분명하고 작동 원리가 잘 파악되지 않는 코드는 혹시 모르니 차단하는 거죠.
면역계가 외래 mRNA에 강한 거부반응을 보이는 것도 같은 이유입니다. 어느 세포에서 나온 건지도 알 수 없는 수상쩍을 RNA 조각이 둥실둥실 떠다니면 십중팔구는 외부에서 침투한 것일 테고, 까딱 내버려 뒀다가는 바이러스가 번식하도록 방치하는 꼴이 될 테니까 눈에 띄는 대로 태워버리는 거죠.
이런 공격을 피하기 위해 화이자나 모더나 백신을 구성하는 mRNA 분자는 '자연스러운' RNA 분자와는 화학적으로 조금 다른 분자를 사용합니다. 면역계에서는 RNA로 인식하지 않지만 리보솜에서는 인식될 수 있도록 하는 거죠. 이를 변형 RNA (modified RNA, modRNA)라고 부르는데요, 인체 면역계에서는 수상쩍은 RNA를 보면 세포 안으로 들어오게 허락해 주지도 않고 태워버리려고 하지만 modRNA는 그렇게까지 경계하지 않아서 세포 안으로 침투해서 단백질을 생산하는 데에도 잘 관여한다고 알려져 있습니다.
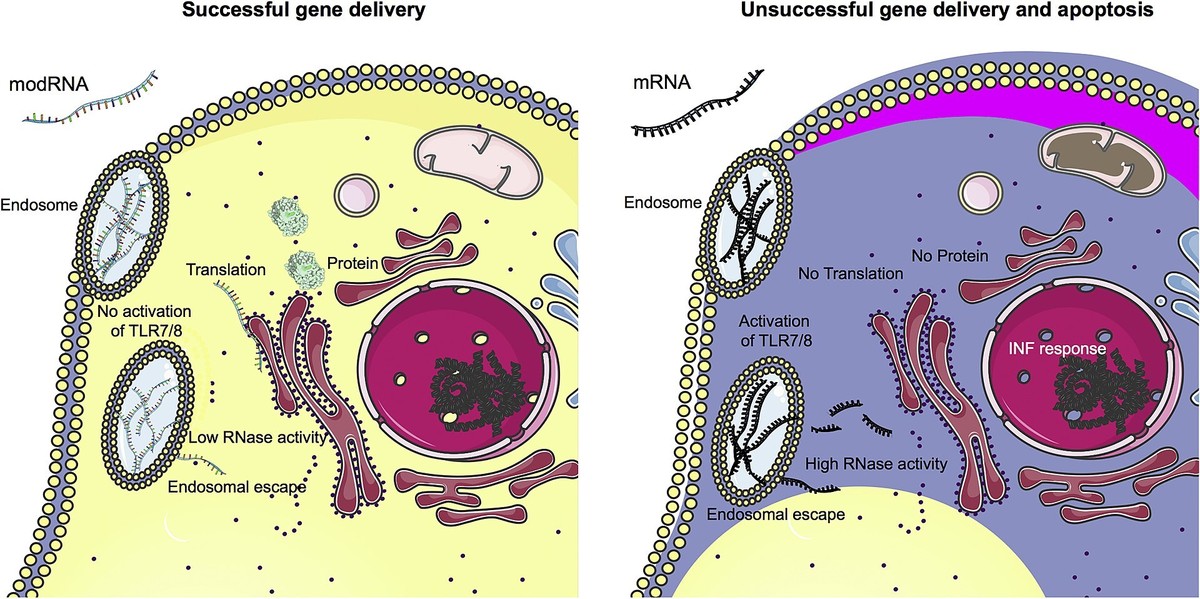
모더나/화이자와 달리, 큐어백의 mRNA 백신은 modRNA를 사용하지 않고 생물체가 사용하는 RNA와 같은 분자를 사용해서 만들어졌습니다. 이유는 여러 가지 있었지만, 일차적으로는 큐어백 측에서 그냥 mRNA를 사용해도 큰 문제가 없을 거라고 판단했던 것도 있고, modRNA가 mRNA에 비해서 훨씬 불안정하기 때문에 일반 mRNA를 사용했을 때 더 높은 온도에서 보관할 수 있다는 것도 있었지요.
수상쩍은 RNA 분자가 혈관을 떠돌아다니면 인체 면역계는 당연히 이걸 퇴치하기 위해 온갖 면역 세포를 불러들이겠지요. 큐어백 연구진의 가설은 '이렇게 면역세포가 잔뜩 모여들면 그만큼 면역 형성도 잘 될 것이다'였어요. 노바백스의 경우에도 일부러 면역반응을 촉진하는 면역보조제(adjuvant)를 섞어 주니까요. 하지만 뚜껑을 열어보니 강화된 면역반응 덕에 면역 기억이 잘 형성되기보다, 몰려든 면역세포들이 수상한 mRNA 분자를 죄다 태워버리는 바람에 정작 스파이크 단백질이 제대로 합성되지 않아서 코로나19에 대항해 훈련할 기회가 오히려 부족해진 것 같습니다.
큐어백 측은 보도자료에서 "모더나와 화이자의 임상시험 당시와 달리 변종 바이러스가 너무 많이 돌아다니고 있어서 백신의 효과가 떨어진 것 같다"며, 임상에서 검출된 코로나19 감염자 중 변이가 일어나지 않은 오리지널 코로나19 바이러스에 감염된 사람은 한 명뿐이었다고 변명했습니다. 하지만 이전 글에서 소개했다시피 모더나와 화이자의 mRNA 백신이 변이 바이러스에 대해서도 강력한 방어력을 발휘하는 걸 보면 별로 설득력이 있지는 않죠.
mRNA 기술의 초석을 놓은 드류 와이즈만 교수도 비슷한 의견입니다. 와이즈만 교수의 핵심 아이디어가 바로 면역계를 회피하면서도 단백질을 생산할 수 있도록 슈도-RNA를 도입하는 거였는데, 큐어백에서 이 부분을 생략하는 바람에 효과가 나빠졌다는 게 그의 의견입니다.
한편으로, 일부 연구자들은 mRNA 백신의 투여 용량이 부족했기 때문이라는 의견도 내고 있습니다. 큐어백의 임상시험을 주도했던 튀빙겐 의과대학의 페터 크렘스너(Peter Kremsner) 교수가 대표적이지요. 임상 1상을 거쳐 최종적으로 결정된 큐어백 백신의 투여 용량은 12마이크로그램이었습니다. 즉, 백신 1회분을 접종받으면 체내에 큐어백의 mRNA 12마이크로그램을 투여받는 거죠.
이는 모더나(100마이크로그램)나 화이자(30마이크로그램)의 투여량보다 현저하게 낮은 용량입니다. 이것밖에 접종하지 못했던 이유는 큐어백 백신을 고용량으로 맞은 사람들에게서 심한 두통, 오한, 통증 등의 꽤 심한 부작용이 나타났기 때문이에요. 결국 부작용을 피하기 위해 적은 용량만 주사하다 보니 면역반응을 충분히 끌어내지 못한 겁니다. 만약 이 가설이 사실이라면, modRNA가 아닌 일반 mRNA를 사용하는 것 자체는 문제가 되지 않았지만 단순히 투여 용량을 맞출 수 없었던 게 함정이었던 거고요.
하지만 큐어백의 임상은 아직 끝나지 않았습니다. 일단 CVnCoV의 추가적인 임상시험 결과가 몇 주 후에 더 나올 예정이어서 여기서 판도를 바꿀 만한 데이터가 나오는지를 지켜봐야 합니다. 그리고 큐어백은 영국의 제약사 글락소스미스클라인(GlaxoSmithKlein)과 협력하여 2세대 코로나19 mRNA 백신도 준비하는 중인데, 쥐와 원숭이를 대상으로 한 실험에서 CVnCoV보다 10배나 강한 면역반응을 보였다고 해요. 변이 바이러스와의 싸움이 길어지는 와중에, 당장은 실패했다 하더라도 mRNA 백신 기술이 다변화되는 것은 좋은 방향일 겁니다.


의견을 남겨주세요